利用小分子前体在细胞内组装成纳米结构是一种智能策略,其在分子影像和药物递送领域显示出很大优势。小分子容易被细胞摄取,但会很快被清除。纳米结构在细胞中保留时间长,但很难被细胞摄取。小分子在细胞内形成纳米结构的“智能”策略,恰好利用了小分子和纳米结构互补的优势。但由于细胞内存在大量的天然纳米结构,迄今为止,如何把人工形成的纳米结构从细胞内的天然纳米结构中区分出来仍然是一个挑战。
梁高林教授研究团队发展了一种含碘小分子在细胞内自组装成富碘纳米粒子的“智能”策略。合理设计并合成了含碘小分子4-nitrobenzyl carbamate-Cys(SEt)-Asp-Asp-Phe(Iodine)-2-cyano-benzothiazole (NBC-Iod-CBT),当NBC-Iod-CBT进入硝基还原酶高表达的癌细胞后,其双硫键被细胞内谷胱甘肽还原、NBC底物被硝基还原酶酶切,生成活泼中间体Cys-Iod-CBT。两个Cys-Ido-CBTs之间立即发生CBT-Cys点击缩合反生成两亲性的环状二聚体Iod-CBT-Dimer,该二聚体可自组装成纳米粒子Iod-CBT-NPs。
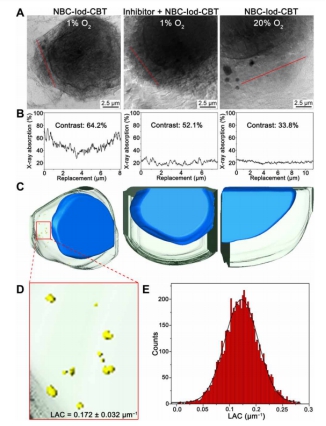
研究过程中,该团队利用国家同步辐射实验室软X射线成像线站在“水窗”波段对未染色的、约10微米厚的冷冻癌细胞开展高衬度、高空间分辨的准自然状态三维成像,直接观察到细胞内富碘纳米粒子Iod-CBT-NPs的形成。并且,线站工作人员利用自主发展的数据分析方法计算了细胞内部纳米粒子的线性吸收系数,帮助用户进一步确定了细胞内部纳米粒子及其分布。该线站发展的线性吸收系数计算方法已经被广泛用于用户实验数据的定量分析。
相关工作以“Directly observing intracellular nanoparticle formation with nanocomputed tomography”为题,于2020年10月23日发表在国际著名学术期刊《Science Advances》上(Sci Adv, 2020, 6, eaba3190. DOI: 10.1126/sciadv.aba3190)。
文章链接:https://advances.sciencemag.org/content/6/43/eaba3190.full


